Um tratamento com células-tronco mesenquimais humanas aumentou em 50% a sobrevida de camundongos com câncer de mama em experimentos realizados na Universidade de São Paulo (USP) e na Universidade Federal de São Paulo (Unifesp).
A pesquisa foi conduzida no âmbito do Centro de Pesquisa sobre o Genoma Humano e Células-Tronco, um dosCEPIDs apoiados pela FAPESP. Os resultados foram divulgados na revista Stem Cells International.
“A terapia com células mesenquimais não curou a doença, mas retardou sua progressão. E aplicamos apenas duas injeções de células-tronco nos animais. É possível que um tratamento continuado, aliado à cirurgia para remoção do tumor, tenha um resultado ainda mais significativo”, comentou Tatiana Jazedje, coordenadora da pesquisa apoiada pela FAPESP.
Encontradas em praticamente todos os órgãos humanos e também de roedores, as células-tronco mesenquimais auxiliam na sobrevivência dos tecidos produzindo diversos fatores que garantem suporte para o crescimento e a diferenciação celular. Embora não tenham a capacidade de se diferenciar em todos os tecidos do corpo como fazem as células-tronco embrionárias, são consideradas interessantes do ponto de vista terapêutico, pois têm propriedades anti-inflamatórias, antiapoptóticas (evitam a morte celular) e imunomoduladoras que estão sendo testadas contra diversas doenças.
Podem ser facilmente obtidas da medula óssea ou do tecido adiposo e expandidas em cultura de laboratório. No caso da pesquisa realizada no IB-USP, foram extraídas de tecido de trompas de falópio humanas descartado após cirurgia de laqueadura.
“Usamos uma linhagem de células mesenquimais que nosso grupo descreveu pela primeira vez em 2009, no Journal of Translational Medicine. Supomos que, pelo ambiente em que são encontradas originalmente, tenham um papel imunomodulador importante na fertilização. Como o câncer de mama é uma doença que afeta predominantemente mulheres, decidimos avaliar o efeito dessas células no tratamento desses tumores”, contou Jazedje.
De acordo com a pesquisadora, os estudos que haviam sido feitos anteriormente por outros grupos com esse objetivo apresentavam resultados contraditórios. Para Jazedje, a explicação está no fato de as metodologias usadas serem muito diferentes, o que impede a comparação.
“Variava a linhagem de camundongos utilizada, a idade dos animais, a forma de administração das células, o estágio da doença em que o tratamento foi iniciado e, além disso, alguns trabalhos usaram roedores imunossuprimidos, o que acredito não ser uma boa opção. Quando o sistema imunológico não funciona, tudo vai pior e não necessariamente por causa das células mesenquimais”, comentou a pesquisadora.
O grupo do IB optou por administrar em camundongos da linhagem Balb-c as células-tronco mesenquimais pela via intraperitoneal, ou seja, por meio de injeções na região do peritônio, a membrana que reveste os órgãos da cavidade abdominal.
Para induzir o câncer, células tumorais da linhagem 4T1 – a mais utilizada em estudos desse tipo – foram aplicadas na gordura mamária dos camundongos. Sete dias após o procedimento, os animais já apresentavam pequenos tumores palpáveis e a terapia foi iniciada.
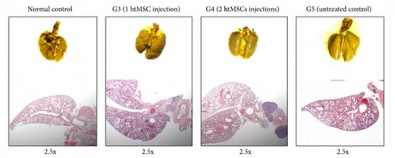
Um primeiro grupo recebeu apenas placebo. O segundo recebeu uma dose das células mesenquimais (1 milhão de células) no sétimo dia após a indução do tumor. O terceiro grupo recebeu duas doses do tratamento, sendo a primeira no sétimo dia e, a segunda, uma semana depois.
Os animais do grupo controle morreram entre 30 e 35 dias depois da indução do tumor. O grupo que recebeu apenas uma dose do tratamento não apresentou diferença estatística significante em relação ao grupo controle. Já os animais tratados com duas doses de células mesenquimais viveram até 45 dias após a indução do tumor, o que representa uma sobrevida 50% maior que a dos camundongos controle.
Em um outro experimento, os pesquisadores misturaram células-tronco mesenquimais e células tumorais. Em seguida, injetaram essa mistura em camundongos sadios da mesma linhagem Balb-c.
“Esses animais morreram apenas 15 dias depois da indução do tumor, ou seja, apresentaram uma evolução clínica muito pior que a do grupo controle não tratado do experimento anterior. Concluímos que, quando é feita essa co-injeção, os fatores liberados pelas células mesenquimais favorecem a proliferação do tumor e a formação de metástase, fazendo o animal morrer prematuramente”, disse a pesquisadora.
Outras fontes
O grupo testou ainda, no mesmo modelo animal do primeiro experimento, o tratamento com células mesenquimais humanas obtidas de medula óssea e de tecido adiposo. No entanto, não foram alcançados nesses casos resultados tão bons quanto o observado com as células extraídas de trompa de falópio.
Ao testar um tratamento com células mesenquimais murinas (extraídas de camundongos), os pesquisadores não observaram aumento na sobrevida. Contudo, houve melhora em outros aspectos, como redução da inflamação pulmonar e menor formação de metástase. Parte desse trabalho foi desenvolvida pela aluna de Iniciação Científica Aline Ribeiro, bolsista FAPESP.
Durante o mestrado de Mayra Vitor Pelatti, realizado sob a orientação de Jazedje, foram feitos experimentos in vitro para tentar desvendar por meio de qual mecanismo o tratamento com células humanas retardou a progressão do tumor no primeiro experimento.
Ao colocar na mesma cultura as células mesenquimais e tumorais, o grupo notou queda na produção da proteína VEGF (Fator de Crescimento Endotelial Vascular, na sigla em inglês), que é importante para a formação de novos vasos sanguíneos que vão nutrir o tumor.
“VEGF é uma citocina fortemente relacionada à angiogênese. Sendo assim, uma diminuição na produção do VEGF pode desacelerar o crescimento tumoral, o que é benéfico ao indivíduo com a doença”, comentou Jazedje.
Na avaliação da pesquisadora, os achados demonstram que a mesma célula mesenquimal pode ter efeito benéfico ou maléfico, dependendo da forma como for administrada.
“Além disso, sabemos que nem todas as células-tronco mesenquimais obtidas de trompas de falópio se comportam da mesma forma. Cada uma tem um perfil diferente, de acordo com a doadora. Existe potencial para serem usadas como coadjuvantes no tratamento do câncer de mama, mas ainda são necessários novos estudos para termos segurança”, avaliou.