Em testes com camundongos, estratégia diminuiu em 74% a formação de lesão aterosclerótica (por acúmulo de placas de colesterol nos vasos sanguíneos) e em 88% a liberação de moléculas inflamatórias
Uma nanoformulação capaz de remover da circulação sanguínea as partículas mais nocivas do “colesterol ruim” – a lipoproteína de baixa densidade eletronegativa (LDL-, na sigla em inglês) – está sendo testada em camundongos por pesquisadores da USP.
O estudo é conduzido na Faculdade de Ciências Farmacêuticas (FCF) da USP, no âmbito de um Projeto Temático da Fapesp, que tem Dulcineia Saes Parra Abdalla como pesquisadora principal. Resultados recentes foram publicados no European Journal of Pharmaceutics and Biopharmaceutics.
“Nossa proposta é criar um sistema para remover essa LDL- da circulação, de modo a impedir que essas partículas interajam com a parede das artérias e induzam a uma resposta pró-inflamatória que contribua para o início e a progressão da lesão aterosclerótica”, contou Dulcineia Abdalla à Agência Fapesp.
De acordo com a pesquisadora, embora toda a fração das lipoproteínas de baixa densidade (LDL) tenha a fama de “colesterol ruim”, a subfração eletronegativa (LDL-) – que inclui partículas modificadas por processos químicos, como oxidação e lipólise – pode ser considerada a mais aterogênica e, portanto, a principal ameaça à saúde cardiovascular.
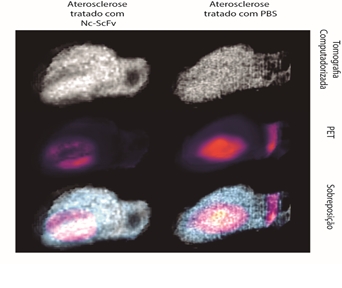
Em testes com camundongos, estratégia terapêutica desenvolvida na USP diminui em 74% a formação de lesão aterosclerótica e em 88% a liberação de moléculas inflamatórias – Imagem: Divulgação via Agência Fapesp
Ao ser reconhecida e internalizada por macrófagos, um tipo de célula do sistema imunológico, a LDL- desencadeia uma resposta inflamatória que aumenta a instabilidade da placa aterosclerótica, contribuindo para a ruptura do ateroma na parede da artéria. Esse processo pode culminar em um evento cardiovascular, como infarto agudo do miocárdio ou acidente vascular cerebral.
“Ao internalizar esses lipídeos modificados, os macrófagos se transformam no que chamamos de células espumosas. O acúmulo dessas células espumosas representa o início da lesão aterosclerótica. Quando esses macrófagos morrem, liberam todo o seu conteúdo de lípides e outros fragmentos celulares, formando uma região necrótica na parede da artéria. Isso atrai ainda mais macrófagos para o local, bem como linfócitos e outros tipos de células de defesa, que passam a liberar mais moléculas inflamatórias, agravando o quadro”, explicou Dulcineia.
Inicialmente, contou a pesquisadora, o objetivo do grupo foi criar uma metodologia para detectar a subpopulação de partículas LDL- em pacientes com dislipidemias, diabete, insuficiência renal crônica e outras enfermidades associadas ao risco cardiovascular. Vale lembrar que os exames convencionais feitos em laboratório medem as lipoproteínas de baixa densidade como um todo, sem discriminar essa subfração mais aterogênica.
“Desenvolvemos anticorpos monoclonais capazes de identificar e se ligar somente às partículas LDL- para fins de diagnóstico. Mas depois pensamos que poderíamos aproveitar essa ferramenta em uma abordagem terapêutica, ou seja, usar esses anticorpos para neutralizar as partículas aterogênicas”, contou Dulcineia.
Traçando a estratégia
Os estudos em andamento usam um modelo experimental de aterosclerose. Camundongos foram modificados geneticamente para não expressar o gene da proteína que atua como receptor para as lipoproteínas da classe LDL. Dessa forma, o “colesterol ruim” se acumula na circulação do animal – simulando casos de hipercolesterolemia familiar. Esse acúmulo leva ao desenvolvimento de lesões ateroscleróticas, no caso dos camundongos principalmente na região do arco aórtico (a parte da artéria aorta que fica dentro do coração). Com menos de dois meses de dieta rica em colesterol, esses roedores desenvolvem aterosclerose.
Inicialmente, o grupo da FCF testou o tratamento com o anticorpo monoclonal inteiro. Mas, ao se ligar ao antígeno (as partículas LDL-), o imunocomplexo formado poderia ser internalizado pelos macrófagos, o que faria aumentar ainda mais a formação de células espumosas e exacerbaria a resposta inflamatória.
“Foi então que pensamos em cortar uma parte do anticorpo e trabalhar apenas com as porções capazes de reconhecer o antígeno. Assim, a porção do anticorpo que se liga aos receptores dos macrófagos – chamada Fe – seria eliminada”, contou Dulcineia.
Por meio de engenharia genética, em parceria com a pesquisadora Andrea Queiroz Maranhão, da Universidade de Brasília (UnB), o grupo desenvolveu um método para expressar em leveduras da espécie Pichia pastoris uma proteína recombinante formada pelas regiões hipervariáveis das cadeias leve e pesada do anticorpo que reconhecem a LDL-, que foram unidas por um peptídeo conector. Essa proteína é chamada pelos pesquisadores de scFv (fragmento variável de cadeia única, na sigla em inglês). Essa parte do trabalho foi desenvolvida durante o mestrado de Soraya Megumi Kazuma, com bolsa da Fapesp.
“O problema é que o scFv é uma molécula pequena com tempo de meia-vida na circulação sanguínea baixo, quando comparado ao do anticorpo monoclonal completo. Então nossa estratégia foi incorporar o scFv em uma nanocápsula para aumentar o tempo de vida na circulação e permitir, no futuro, a liberação de fármacos no ateroma de forma dirigida”, revelou a pesquisadora.
Essa parte do trabalho contou com a colaboração de Adriana Raffin Pohlmann e Silvia S. Guterres – ambas da Universidade Federal do Rio Grande do Sul (UFRGS). Duas patentes referentes à nanoformulação já foram depositadas no Instituto Nacional da Propriedade Industrial (Inpi) pelos pesquisadores.
De acordo com o relato de Dulcineia, a nanoformulação contém nanocápsulas poliméricas de multicamadas, ou seja, há um núcleo lipídico, onde é possível colocar fármacos lipossolúveis, recoberto por múltiplas camadas nas quais é possível acrescentar outros fármacos ou moléculas para o direcionamento do fármaco ao alvo terapêutico.
“Nossa estratégia foi colocar o scFv na superfície da nanopartícula, para direcioná-la à LDL- presente na circulação. Dessa forma a LDL- ligada à nanoformulação não seria internalizada pelos macrófagos e o scFv também não se ligaria a essas células via receptores Fe, que seriam usados pelo anticorpo completo. Isso reduziria o processo de acúmulo de colesterol proveniente da lipoproteína modificada pelo macrófago e, consequentemente, diminuiria a formação das células espumosas e a liberação de mediadores pró-inflamatórios na parede arterial”, explicou a pesquisadora
Prova de conceito
No modelo experimental, os pesquisadores testaram um protocolo de prevenção da aterosclerose com a nanoformulação. O trabalho foi feito durante o doutorado de Marcela Frota Cavalcante, bolsista Fapesp. Uma dose foi injetada nos camundongos sete dias antes de ter início a dieta rica em colesterol. Outras quatro doses foram aplicadas ao longo de 28 dias de dieta com 0,5% de colesterol. No final desse período, foi feita uma análise histológica da região do arco aórtico.
Em comparação com os animais do grupo controle – que em vez da nanoformulação receberam apenas placebo – os camundongos tratados apresentaram uma área com lesão aterosclerótica 74% menor. Também foi observada no tecido uma quantidade 68% menor de interleucina-1 beta (IL-1β) – citocina pró-inflamatória liberada pelos macrófagos.
“A liberação dessa citocina IL-1β, dentre outras, é um fator importante para aumentar a atividade inflamatória da placa aterosclerótica e isso é mais problemático do que o tamanho da lesão em si, pois aumenta o risco de ruptura do ateroma e de formação de trombo. Por isso, atualmente, a principal estratégia terapêutica tem sido combater a inflamação nas placas ateroscleróticas”, explicou Dulcineia.
A nanoformulação, segundo a pesquisadora, atua em duas frentes: retira da circulação um estímulo pró-inflamatório – a lipoproteína modificada – e minimiza o acúmulo de lípides no vaso sanguíneo. Diminui, portanto, tanto o tamanho da lesão quanto a atividade inflamatória na placa.
Atualmente, o grupo vem fazendo estudos com camundongos com o intuito de verificar quanto tempo a nanoformulação permanece no organismo antes de ser metabolizada e para onde ela direciona as partículas LDL-. Para isso, estão sendo usadas técnicas de imagem molecular, como tomografia por emissão de pósitrons e tomografia computadorizada. O trabalho conta com a colaboração de pesquisadores do Instituto de Pesquisas Energéticas e Nucleares (Ipen). Os resultados devem ser divulgados em breve.
O artigo A nanoformulation containing a scFv reactive to electronegative LDL inhibits atherosclerosis in LDL receptor knockout mice (doi: 10.1016/j.ejpb.2016.07.002) pode ser lido emwww.sciencedirect.com/science/article/pii/S0939641116302612.
Karina Toledo/Agência Fapesp